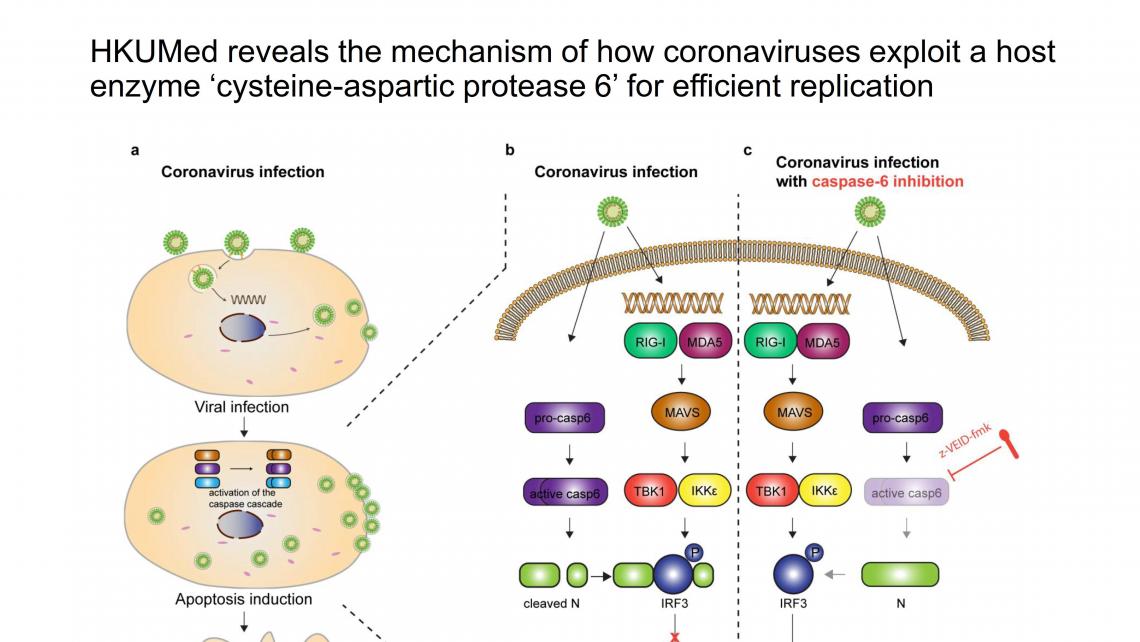
香港大学李嘉诚医学院(港大医学院)临床医学学院微生物学系研究人员发现冠状病毒如SARS-CoV-2,SARS-CoV-1和MERS-CoV等,皆可利用宿主细胞蛋白酶「半胱天冬酶-6(caspase-6)」进行更有效的复制,并阐释其相关原理。研究结果经同行评审,已于《自然》杂志发表(按此浏览期刊文章)。
研究背景
当冠状病毒进入宿主细胞后,病毒核糖核酸(RNA)会刺激受感染细胞分泌干扰素。干扰素能够抑制病毒在受感染细胞内的复制,并能降低周围未感染细胞被其他病毒感染的风险。同时,宿主细胞将经历凋亡过程,使细胞不会成为生产数百万病毒的工厂。因此干扰素反应和细胞凋亡反应是人和动物细胞防御病毒的两个最重要的机制。
人和动物细胞内的细胞蛋白酶「半胱天冬酶-6」负责执行细胞凋亡程序,可以通过消除受感染的细胞,从而控制病毒的复制。港大医学院研究团队在一系列细胞系、离体肺组织、小肠类器官和动物模型中,研究半胱天冬酶-6对冠状病毒复制的影响。团队发现在细胞系、离体肺组织和小肠类器官的实验中,半胱天冬酶-6抑制剂或半胱天冬酶-6的剔除可有效降低冠状病毒的复制能力。相反,在过度表达「半胱天冬酶-6」的细胞中,冠状病毒的复制能力显著提高。
研究结果
在小鼠模型中,半胱天冬酶-6抑制剂显著降低了MERS-CoV(MERS-CoVMA)的复制能力,小鼠存活率则由33.3% 提升至80%。而在半胱天冬酶-6基因已被剔除的小鼠中,MERS-CoV复制能力和引致的肺部损伤水平也显著降低。同样地,在仓鼠模型中,半胱天冬酶-6抑制剂显著降低了SARS-CoV-2复制能力,同时改善了肺部炎症反应和损伤水平。
干扰素反应是宿主细胞最重要和最直接的抗病毒防御机制。团队的研究进一步证明,半胱天冬酶-6可裂解冠状病毒核壳蛋白(nucleocapsid,简称N),产生的核壳蛋白片段可以与抗干扰素调节因子-3(Interferon Regulatory Factor 3,IRF-3)结合,并阻止其进入细胞核以启动干扰素反应;通过停止干扰素反应,从而加强病毒的复制能力。
研究意义
是次研究首次揭示了何以冠状病毒是非常成功的致病病毒,因为冠状病毒能够利用宿主被激活凋亡反应所产生的半胱天冬酶-6,提升有效的病毒复制能力。由于细胞凋亡是人体对抗病毒感染的第一道天然免疫屏障,研究也揭示了冠状病毒可以反利用「人体抗病毒免疫屏障」,促进自身复制,并详细解释其促进病毒复制的机制。这为治疗高致病性冠状病毒提供了潜在的干预目标,及可能选择使用的化合物。研究结果进一步提出裂解后的病毒蛋白可发挥免疫对抗作用,为病毒蛋白研究及相关药物研究提供了创新的研究方向。
研究团队
是次研究由研究团队由港大医学院临床医学学院微生物学系助理教授朱轩博士、临床副教授陈福和医生及香港大学新发传染性疾病国家重点实验室主任、中国工程院院士、港大医学院临床医学学院微生物学系讲座教授暨霍英东基金教授(传染病学)袁国勇教授领导。
详情:https://www.hku.hk/press/press-releases/detail/c_24882.html